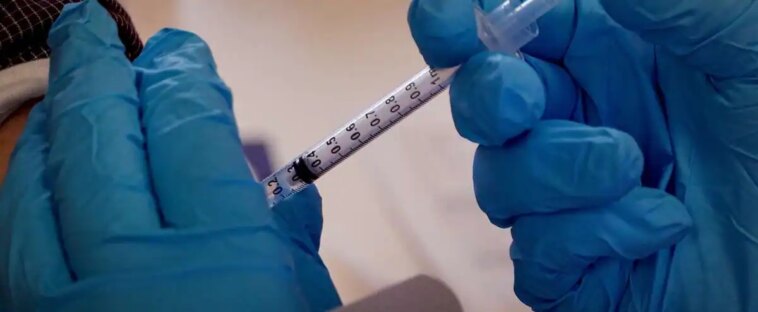
Les nouveaux vaccins contre la COVID-19 commencent à être autorisés à travers le monde. Comment fonctionnent-ils, qui les fabrique? Le point sur ces nouveaux sérums.
• À lire aussi: C’est fini le télétravail pour les enseignants ayant des symptômes de COVID-19
Une adaptation à l’évolution des virus
Le virus de la maladie COVID-19, le SARS-CoV-2, a une capacité de mutation, comme les autres virus. C’est un mécanisme naturel: les virus se multiplient et des modifications génétiques accidentelles peuvent avoir lieu, au gré de la réplication de leur ADN.
Les premiers vaccins ont été développés à partir de la souche initiale, dite de Wuhan. Depuis, d’autres variants ont vu le jour, comme Delta ou Omicron. Ce dernier représente en fait une famille de variants, dont plusieurs sous-lignages circulent actuellement, tel BA.1.
Omicron et ses sous-variants ont été dominants tout au long de 2022, prenant rapidement la place des variants précédents Alpha et Delta. Aujourd’hui, c’est essentiellement le sous-variant BA.5 d’Omicron qui domine en Europe et aux États-Unis. C’est pour mieux répondre à ces mutations que les groupes pharmaceutiques adaptent leurs vaccins.
Un concept qui n’est pas neuf: dans le cas de la vaccination contre la grippe par exemple, des vaccins quadrivalents –développés avec des composants de deux souches du type influenza A et de deux virus influenza de type B– sont utilisés.
Des vaccins bivalents
Dans le cas du Covid, des vaccins dits bivalents sont conçus dans le même but: éduquer le système immunitaire à reconnaître plusieurs attaquants. Le tandem américano-allemand Pfizer-BioNtech a ainsi adapté son premier vaccin (Comirnaty) contre la souche de Wuhan pour l’arrivée d’Omicron. Il propose désormais en dose de rappel un vaccin bivalent «Omicron BA.1», qui contient à la fois de l’ARN messager (ARNm) du virus original SARS-CoV-2, et de l’ARN messager spécifique au variant Omicron BA.1.
Ce sérum a été autorisé par l’Agence européenne du médicament début septembre. Des centaines de millions de doses seront prêtes cette année, indique Pfizer.
Spikevax, le vaccin de la biotech américaine Moderna, a également été adapté sous la forme d’un vaccin bivalent contre BA.1, sur le même principe que celui de Pfizer. Ce sérum «Originel/Omicron BA.1» a été approuvé au Canada ainsi que par l’Agence européenne du médicament début septembre.
En plus de Moderna et de Pfizer/BioNTech, d’autres vaccins bivalents sont en préparation. C’est le cas notamment d’un candidat-vaccin des laboratoires français et britannique Sanofi et GSK ciblant les souches Delta et Bêta.
L’arrivée des sous-variants BA.4 et BA.5
Les laboratoires travaillent à d’autres vaccins bivalents, ciblant spécifiquement, en plus de la souche originale, les sous-variants d’Omicron, BA.4 et BA.5, devenus dominants.
Pour l’Europe, Pfizer et BioNTech ont une longueur d’avance. Ils ont ainsi reçu fin août une autorisation d’urgence de la FDA pour leur vaccin bivalent contre BA.4 et BA.5.
Ils ont en outre reçu le feu vert de l’Agence européenne du médicament le 12 septembre.
De son côté, Moderna a également développé un vaccin bivalent ciblant BA.4/5: ce dernier est à ce jour uniquement approuvé aux États-Unis, pas encore dans l’Union européenne. Moderna explique toutefois que son sérum Spikevax bivalent contre BA.1 «démontre (…) aussi une réponse plus élevée contre les sous-lignages d’Omicron BA.4/5» par rapport au vaccin de première génération.
Mais faute de données cliniques complètes, le Pr Antoine Flahaut, directeur de l’Institut de santé globale de l’université de Genève, se dit prudent quant à la «supériorité» des nouveaux vaccins bivalents par rapport aux premières formules.
Quels sérums pour la campagne vaccinale d’automne?
La France a réalisé des commandes de plusieurs millions de vaccins bivalents Wuhan/BA.1 et Wuhan/BA.5 auprès de Pfizer/BioNTech et Moderna, indique la Direction générale de la santé à l’AFP. Ces doses seront mises à disposition des officines et centres de vaccination dès que la Haute autorité de santé (HAS) aura rendu son avis sur la place de ces nouveaux vaccins dans la stratégie vaccinale française.
Des commandes auprès des laboratoires Sanofi (monovalent Bêta) et espagnol Hipra (bivalent Alpha-Bêta), dont les vaccins sont encore étudiés par l’Agence européenne du médicament, ont également été passées, mais ne sont pas attendues avant la fin de l’année, précise également la DGS.
La 4ème dose reste recommandée aux personnes les plus à risque de développer des formes graves de la COVID-19, leurs proches et quelques professions du secteur médico-social, particulièrement exposées au virus.